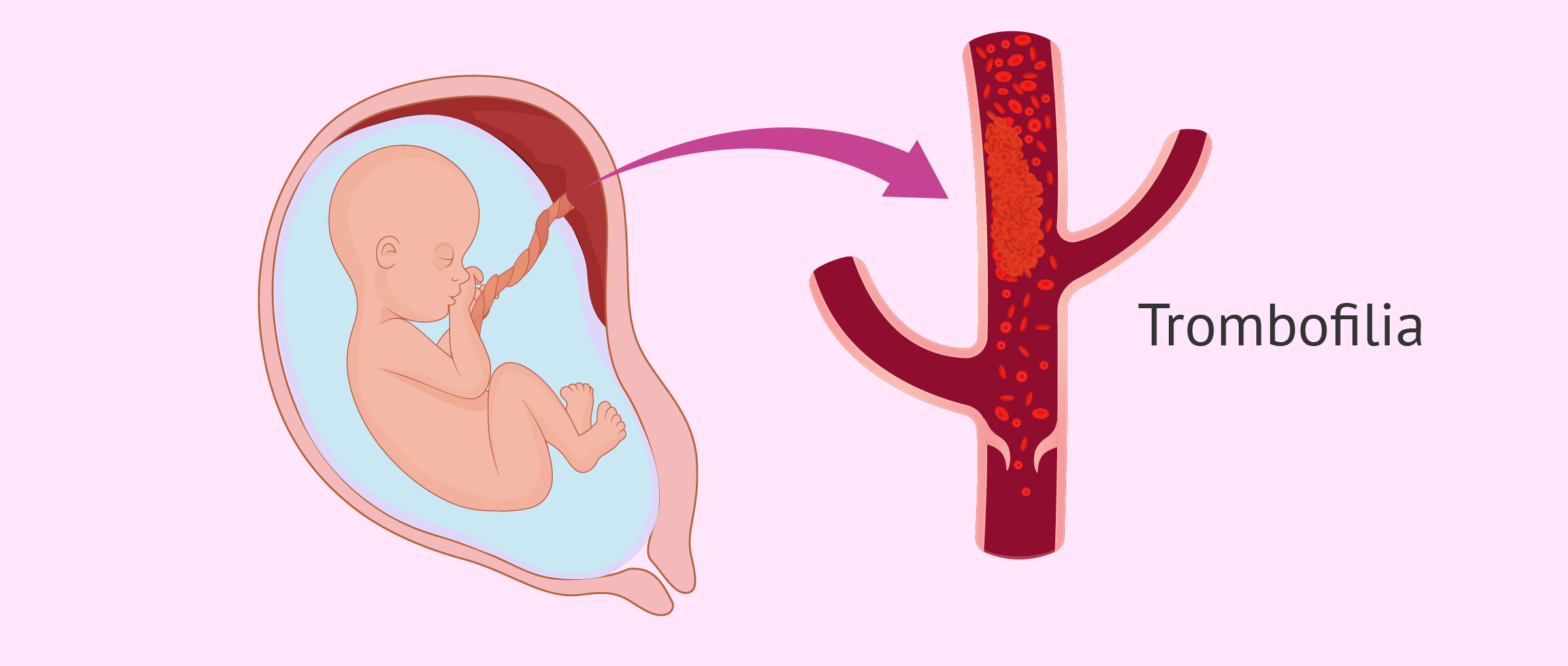
1-بررسی موتاسیون G20210A در ژن پروترومبین
پروترومبین یک پیش ساز ترومبین بوده و تحت اثر آنزیمهای سرین پروتئاز که یک آنزیم کلیدی در سیستم هموستاز و یا انعقاد بدن می باشد، این تغییرات صورت می گیرد.
شیوع این موتاسیون در جمعیت سفید پوستان، حدود 3 درصد است که نسبتاً بالا بوده و معمولاً این بیماران یک سابقه شخصی و یا فامیلی از یک ترومبوآمبولی وریدی (VTA) می باشد.
جهش پروترومبین G20210A که در منطقه ترجمه نشده ‘ 3 ژن فاکتور II و یا پروترومبین رخ میدهد، همراه با افزایش ابتلا به ترومبوز در جمعیت قفقازی دیده میشود، البته وجود این رابطه در جمعیتهای دیگر هنوز مورد بحث است.
پژوهشها نشان دادهاند که این جهش غالب بوده و فرم هتروزیگوت جهش خطر ابتلا به ترومبوآمبولی وریدی را تا سه برابر افزایش میدهد.
افراد تا موتاسیون های هموزیگوت ، ریسک بالاتری از افراد هتروزیگوت دارند.
سطح پروترومبین در افرادی که واریانت هتروزیگوت ژن پروترومبین G20210A را دارند تقریباًَ 25% بیش از میانگین سطح پروترومبین در افراد طبیعی است.
بعضی از پژوهش ها نشان میدهد که جهش G20210A برخلاف شیوع بالا در کشورهای غربی، در کشور ما از شیوع کمی برخوردار است(1.7% در مقابل جمعیت قفقازی که حدود 18% است).
در حالی که مقاومت به پروتئین C فعال شده ( APC ) شایع میباشد.
در حالیکه یک مطالعه دیگر در جنوب ایران توسط دکتر محدثه عرب نژاد و همکاران درسال 94 ، ﻓﺮاواﻧﻲ ژﻧﻮﺗﻴﭗ GG، GA ﺑﻪﺗﺮﺗﻴﺐ 9/97% و 1/2% ﺑﻪدﺳﺖ آﻣﺪ.
و ﻧﺘﺎﻳﺞ پژوهش فوق نشان می دهد که کمترین فرکانس آللی در این جمعیت بالاتر از فراوانی این آلل در جمعیت ایران و اروپا است؛ اما مشابه فراوانی این آلل در جمعیت غرب ایران، ایرانیان یهودی، آمریکا، ایرلند، تونس و بحرین است.
نحوه ریپورت در افراد نرمال:
Homogzygous Wild Type (Normal)
2- فیبرینوژن بتا (Beta Fibrinogen)
فیبرینوژن یا فاکتور 1 انعقادی، یک گلیکو پروتئین محلول در پلاسما است که در آبشار انعقاد توسط ترومبین به رشتههای فیبرین تبدیل میشود.
پلیمورفیسمهای متعددی بر روی ژن زنجیره بتا یا ژن FGB مطالعه شدهاند و پلیمورفیسم پروموتری (rs1800790) G455A، ارتباط معناداری با سطح فیبرینوژن نشان داده است.
به این فیبرینوژن بتا و یا Beta Fibrinogen گفته می شود.
وجود این پلی مرفیسم سبب افزایش 7 الی 10% غلظت پلاسمایی فیبرینوژن شده و در نتیجه می تواند باعث افزایش قابلیت انعقاد خون (هایپر کوآگولابیلیتی) در خون شده و در نتیجه زمینه رسوب فیبرین را در داخل عروق را افزایش دهد.
آلل G بعنوان یک آلل نرمال شناخته می شود و آلل A باعث افزایش ریسک تشکیل ترومبوز می شود.
بعبارت فرم هموزیگوت این آلل ریسک انفارکتوس قلبی و بیماریهای عروق کرونر قلب و یا (coronary artery disease (CAD را افزایش می دهد.
3- کمبود مادرزادی فاکتور XIII
کمبود مادرزادی فاکتور XIII، یکی از اختلالات انعقادی نادر است که می تواند منجر به سقط مکرر شود.
این اختلال دارای شیوع 1 در هر 1 تا 3 میلیون نفر میباشد.
کمبود این فاکتور موجب بروز تظاهرات بالینی دیگری نظیر خونریزی مغزی، سقط جنین و خونریزی تاخیری میگردد.
این بیماری به صورت خونریزی خود به خودی و تأخیری در حضور تست های انعقادی طبیعی تظاهر می یابد.
خونریزی از بند ناف به عنوان شایعترین علامت بالینی اولیه در این بیماران گزارش شده است.
هماتوم و خونریزی طولانی از محل زخم علایم بالینی شایع دیگر این بیماران هستند.
زنان مبتلا به این بیماری علاوه بر قاعدگی شدید و طولانی، در معرض خطر عوارض مختلف بارداری از جمله سقط راجعه می باشند.
وجود واریانت هموزیگوت V/V با کاهش ریسک اختلالات ترومبوآمبولیک همراه است، اما واریانت های V/L و L/L نقشی در کاهش ریسک اختلالات ترومبوآمبولیک ندارند.
همینطور در مطالعات مختلف مشخص شده که شیوع پلی مرفیسم G103T، در افرادیکه سابقه سقط مکرر داشته اند بصورت معنی داری بالاتر بوده است.
4- فاکتور پنج لیدن Factor V Leiden = FVL
فاکتور V Leiden در واقع جزو یک سری اختلالات انعقادی خون است که در نتیجه ی ایجاد جهش در یکی از فاکتورهای خون به نام فاکتور پنج روی داده و به این فاکتور موتاسیون یافته فاکتور V Leiden می گویند و باعث افزایش غیر طبیعی ایجاد لخته و انسداد عروق می گردد.
این موتاسیون سبب می شود که فاکتور پنچ در مقابل قابلیت پروتئولیتیک پروتئین C فعال شده، مقاومت بیشتری نشان دهد.
در واقع پروتئین C فعال شده بعنوان یک فاکتور ضد انعقادی با شکستن فاکتورهای 5 و 8 فعال شده ، باعث مهار فرآیند انعقاد شده و در نتیجه یک تعادلی در بدن بین فعالیت انعقادی ایجاد می کند (در غیر اینصورت فرایند تشکیل لخته ادامه یافته و منجر به ایجاد لخته های غیر ضروری در سیستم گردش خون می شود).
در بسیاری از افراد دارای این اختلال، ایجاد لخته ی غیر طبیعی هرگز اتفاق نمی افتد ولی در برخی موارد وجود این جهش آثار زیان باری بر سلامت فرد خواهد داشت.
جهش V Leiden در هر دو جنس مشاهده می شود اما زنان در مواقع بارداری و یا در وضعیت دریافت استروژن بیشتر در معرض ایجاد لخته های غیر طبیعی می باشند.
در چنین افرادی مصرف داروهای ضد انعقاد می تواند بسیار موثر باشد.
وجود جهش V Leiden در اغلب افراد بدون علامت است اما ایجاد ترومبوز می تواند به عنوان اولین نشانه این اختلال تلقی شود.
علائم و نشانه های این اختلال
1- ایجاد لخته در وریدهای عمقی (DVT):
ایجاد لخته در وریدهای عمقی اغلب بدون علامت است اما گاهی با ایجاد تورم در ناحیه مچ پا همراه است
از دیگر نشانه های ترومبوز در وریدهای عمقی عبارتند از:
درد
تورم
قرمزی و گرمی
وجود لخته در زیر پوست:
از نشانه های این عارضه که ترومبوز سطحی وریدی و یا ترومبوفلبیت نامیده می شود می توان به
ایجاد قرمزی
گرمی
درد و گزگز در اطراف عروق واجد لخته را اشاره کرد.
ایجاد لخته در ریه:
ایجاد لخته در ریه که به نام آمبولی ریوی شناخته می شود، با حرکت لخته از سمت راست قلب و وارد شدن به ریه ایجاد می شود که می تواند کشنده باشد.
نشانه های آمبولی ریوی عبارتند از:
تنگی نفس ناگهانی
درد قفسه سینه به هنگام نفس کشیدن
سرفه همراه با خلط خونی
افزایش ضربان قلب
علل ایجاد انعقاد
به طور طبیعی ایجاد لخته جهت ممانعت از خون ریزی در موارد آسیب به عروق ایجاد می شود. انعقاد از طریق واکنش شیمیایی بین پلاکت ها و فاکتورهای انعقادی انجام می شود.
فاکتورهای ضد انعقاد از تشکیل بیش از حد لخته جلوگیری می کنند.
پروتئین های ضد انعقاد با شکستن فاکتورV و VIII (پنج و هشت فعال شده) سبب حفظ تعادل در مکانیسم انعقاد می گردند.
شکستن فاکتور V Leiden سخت تر از شکستن فاکتور V است در نتیجه احتمال لخته شدن خون در افراد دارای فاکتور V Leiden افزایش می یابد.
عوامل تشدید کننده
سابقه ی خانوادگیV Leiden امکان ابتلا به این جهش را افزایش می دهد همچنین این جهش در 6% مردان و زنان سالم نژاد اروپایی و سفید پوست دیده می شود.
عوارض وجود فاکتور V Leiden
فاکتور V Leiden با عوارض ناشی از لخته شدن خون مرتبط است که از این بین می توان به موارد زیر اشاره کرد:
عوارض در دوران بارداری:
بسیاری از زنان دارای جهش فاکتورV دوران بارداری طبیعی را سپری خواهند کرد اما این جهش می تواند سبب افزایش خطر سقط جنین و سایر عوارض دوران بارداری مانند فشار خون دوره بارداری (پره اکلامپسی)، رشد آهسته جنین و جدایی زود هنگام جفت از دیواره رحم شود.
ترومبوز وریدی عمقی(DVT) :
افراد دارای فاکتور V Leiden بیش از سایر افراد در معرض ایجاد لخته در عروق می باشند.
آمبولی ریوی:
ترومبوز وریدی عمقی امکان ایجاد لخته در مغز و ریه را افزایش می دهد، آمبولی ریوی که با علائمی همچون تنگی نفس یا درد قفسه سینه همراه است میتواند کشنده باشد.
توجه: در صورتی که زنان مبتلا به فرم هتروزیگوت این جهش باشند در صورت استفاده از استروژن و یا قرص های ضد بارداری خوراکی، خطر تشکیل ترومبوز تا 80 برابر افزایش می یابد.
تشخیص
در صورت وجود سابقه لخته شدن غیرطبیعی خون، سابقه سقط جنین و سابقه خانوادگی بیماری های ناشی از لخته شدن شدن خون، آزمایشات مربوط به تشخیص جهش V Leiden از سوی پزشک درخواست می گردد.
این آزمایشات عبارتند از:
1- روش انقعادی
تست مقاومت در برابر پروتئین C فعال شده (Activated Protein C Resistance = APCR): فاکتور C یک پروتئین ضد انعقاد است که عملکرد آن در کنترل فاکتور V و در نتیجه تنظیم سیستم انعقادی موثر می باشد.
چنانچه در فرد جهش فاکتور V Leiden وجود داشته باشد، مقاومت به فاکتور C فعال شده در خون مشاهده می شود.
در افراد طبیعی نسبت مقاومت به پروتئین C فعال شده معمولاً بیشتر از 2 است، در حالیکه در افرادیکه فاکتور V لیدن دارند این نسبت کمتر از 2 است.
هرگاه تست فوق غیرطبیعی بود باید به روش ژنتیکی با استفاده از تست PCR که استاندارد طلایی تشخیص این اختلال است، وجود موتاسیون در فاکتور V مورد تایید قرار گیرد.
2- انجام آزمایش ژنتیک: افرادی که به طور ارثی دارای یک نسخه از ژن فاکتور V Leiden هستند (فرم های هتروزیگوت)، 3 تا 8 برابر و افراد واجد 2 نسخه از این ژن (فرم های هموزیگوت) تا 50 برابر بیشتر از سایر افراد به آمبولیسم عروقی مبتلا می شوند.
بررسی ژنتیکی V Leiden علاوه بر تشخیص این اختلال می تواند ژنوتایپ بیمار و در نتیجه میزان ابتلا به آمبولیسم عروقی در فرد را تعیین کند.
فرم نرمال فاکتور V را Homozygous wild type می گویند.
5- تست PAI-1 و یا بررسی پلی مرفیسم مهار کننده فعال کننده پلاسمینوژن
پروتئین PAI-1 یا E1 Serpin پروتئینی اسـت با وزن مولکولی تقریباً 50kd کـه بـه وسـیله ژن E1 Serpin کـد مـی شـود و به عنـوان اولیـن تنظیم کننـده فعالیت پلاسمینوژن شـناخته شـده اسـت.
ژن مربوطه روی کروموزوم 7 قـرار گرفته اسـت و به عنـوان یک جلوگیری کننده سـرین پروتئینـاز (سـرپین) و جلوگیـری کننـده اصلـی فعالیـت پلاسمینوژن بافتی (TPA) و یوروکینـاز می باشد.
پروتئین PAI-1 بــه وسـیله ســلول هــای اندوتلیـال (ســلول هــای پوشـش دهنده داخلــی رگهــای خونــی) آزاد مــی شــود، ولــی بــه وسـیله انــواع بافــت هــای دیگــر مثـل بافــت چربـی نیـز ترشـح مـی گـردد.
سـطح بالای PAI نتیجـه کمبـود فعالیـت پلاسـمینوژن و همـراه بـا افزایش اسـتعداد ایجـاد ترومبـوز مـی باشـد.
سـطح بـالای خونـی PAI در ترومبوفیلـی هـای دیگـر و سـایر بیمـاری هـا نیز مشـاهده میشـود
پلی مورفیسم ژن PAI
پلــی مورفیسـم 4G/5G در پروموتـور ژن PAI یکــی از واریته هـای توالـی DNA مــی باشــد کــه از نظـر عملکـردی در تنظیـم بیــان ژن PAI نقــش مهمــی دارد.
رونویسـی آلــل 5G کمتـر انجـام مــی شــود، بنابرایـن بالاتریـن سـطح PAI در ژنوتایپهـای 4G/4G و پایین ترین سـطح در ژنوتایـپ هــای 5G/5G مشـاهده میشـود.
بنابراین ژنوتایپ 5G/5G به نظر می رسد که نرمال باشد و ژنوتایپهای 4G/5G و 4G/4G منجر به افزایش ریسک ترومبوز می شوند.
مقـدار بـالای PAI تولیــد شــده در اثـر وجـود آلــل 4G میتوانــد سـبب افزایــش تولیــد لختــه شـود، چــون در سیسـتم فیبرینولیـز و انعقـاد اختلال ایجـاد کــرده و میتوانــد باعـث ترومبـوز و پیــر شـدن زودرس جفـت و ایجـاد سـقط جنیـن گـردد.
افرادی که باید برای انجام تست مراجعه کنند:
1 . افراد با سابقه ترومبوز وریدی
2 . زنان با سقط های مکرر
3 . افـراد بــا سـابقه بیماریهـای مزمـن مثـل ســکته قلبــی
4 . بیماریهـای عـروق محیطــی بــه ویـژه بیماریهـای انسـدادی عـروق
6- تست MTHFR
اصطلاح MTHFR نام اختصاری آنزیم متیلن تترا هیدروفولات ردوکتاز می باشد که نقش محوری در متابولیسم فولات، متیونین و هموسیستئن دارد.
آنزیم MTHFR یک فرم از فولات را به فرم دیگری از آن تبدیل می کند و همچنین بخشی از فرآیند تبدیل هموسیستئین به متیونین می باشد.
متیونین بخش مهمی از ساختار مولکولی بسیاری از پروتئین ها است.
هموسیستئن پلاسما یک آمینو اسید بالقوه سمی است که افزایش آن به علت اثرات پاتولوژیک منفی که بر روی آندوتلیوم عروق، آتروژنسیس (رسوب پلاک های چربی در سطح داخلی سرخرگ قلب) و فعالیت فاکتورهای انعقادی V و VIIIمی گذارد، منجر به افزایش سطح ترومبین، تجمع پلاکت ها و در نتیجه ترومبوز وریدی می شود.
در اصطلاح گفته می شود که هموسیتئین بطور مستقیم می تواند عوارض عروقی که منجر به جراحت شود ایجاد کند.
هموسیستئین با ایجاد جراحتهای بسیار کوچک در سطح سلولهای آندوتلیال، سبب آغاز فرآیند انعقاد میشود و در نتیجه به عنوان مهمترین مارکر بیماریهای عروق کرونر، مغزی و محیطی شناخته شده است.
بنابراین با تبدیل این آمینو اسید به متیونین در بدن اثرات سمی آن خنثی می شود.
ژن MTHFR بر روی بازوی کوتاه کروموزوم شماره یک قرار دارد.
موتاسیون در این ژن سبب می شود که عملکرد این آنزیم کاهش یابد.
بیش از 50 واریانت MTHFR وجود دارد اما دو واریانت اصلی، واریانت هایC677T (جهش در موقعیت نوکلئوتیدی 677 و تبدیل سیتوزین به تیمین) و A1298C (جهش در موقعیت نوکلئوتیدی 1298 و تبدیل آدنین به سیتوزین) هستند، که اهمیت بیشتری داشته و معمولا در تست های آزمایشگاهی روتین مورد بررسی قرار می گیرند.
این دو موتاسیون باعث کاهش شدید فعالیت آنزیم MTHFR و در نتیجه افزایش سطح هموسیستئنی می شود.
اشخاص مبتلا به واریانت C77T به میزان 40 تا 60 درصد برای تولید موثرترین شکل فولات به نام ” متیل فولات ” ناتوان هستند.
میتل فولات ماده ی مغذی، حیاتی و موثر برای تولید منتقل کننده های عصبی، نظم DNA، ایمنی و سیستم قلبی و عروقی است.
متیل فولات به شیوه ای غیر مستقیم بر میزان هورمون ها و سم زدایی بدن تاثیر می گذارد.
واریانت C677T با بیماری کاردیوواسکولار زودرس (early cardiovascular disease) و سکته مغزی (stroke) در ارتباط می باشد و واریانت A1298C با تعدادی از بیماریهای مزمن مثل فایبرومایالجیا (fibromyalgia) و افسردگی (depression) در ارتباط است.
افراد هموزیگوت ژن C677T در نوزادان با افزایش خطر ابتلاء به نقص لوله عصبی (spina bifida) همراه است.
در افراد هتروزیگوت که دارای دو آلل C677T و A1298C می باشند نیز خطر افزایش ابتلا به نقص لوله عصبی وجود دارد.
جهش در ژن MTHFR همچنین می تواند با سقط جنین مرتبط باشد.
در سقط مکرر فاکتورهای ریسک متعددی دخالت دارند و عوامل ژنتیکی به خصوص فاکتور های ترومبوفیلی (لخته دوستی) به عنوان یکی از دلایل سقط مکرر می توانند مطرح باشند زیرا سلامت جنین ارتباط مستقیم با گردش خون مادر دارد و هر عاملی که باعث اختلال در این ارتباط شود می تواند برای جنین زیان آور باشد.
به نظر می رسد که ایجاد لخته نابجا یا ترومبوز می تواند در مویرگ های جفت باعث اختلال در روند تبادلات مواد بین مادر و جنین شده و نهایتاً منجر به سقط گردد.
چگونگی تاثیر این اختلال بر قدرت باروری
ژن MTHFR تولید کننده ماده ای به نام اختصاری (SAMe s- adenosylmethionine) است.
SAMe برای تولید مواد مغذی به نام CoQ۱۰، کارنتین و کراتین ضروری است.
در اغلب موارد کاهش قدرت باروری، فرد دچار کمبود این مواد بوده و برای کسانی که تحت درمان های ناباروری قرار دارند اغلب به صورت مکمل تجویز می گردند.
شیوع
شایعترین واریانت این ژن یعنی واریانت C677T در 5 الی 10 درصد سفید پوستان اروپایی دیده می شود و در بیمارانی که مبتلا به سقط مکرر، بیماریهای شریان کرونر قلب، بیماریهای شریانی و مبتلایان به ترومبوآمبولی وریدی شیوع بیشتری دارد.
کاربردهای بالینی:
1- آنالیز مستقیم موتاسیون MTHFR C677T در بیماران مبتلا به اختلالات شریان کرونری، نقص میوکارد حاد، بیماری شریان عروق محیطی، سکته مغزی (stroke) و ترومبوآمبولیسم سیاهرگی که سطوح افزایش یافته ای از هموسیستئن یا متیونین غیرطبیعی دارند.
2- ردیابی جهش MTHFR C677T در خانم هایی با سابقه سقط های مکرر.
فرم نرمال این دو موتاسیون را homozygous wild type می گویند.
7- تست بررسی آنتی ژنهای پلاکتی و یا HPA-1 (Human platelet antigens)
اتصال پلاکتی و در نتیجه شروع پروسه انعقاد سبب آسیب اندوتلیال شده و در نتیجه آسیب عروقی ایجاد شده ، سبب بروز شیوع بیشتر رخدادهای ترومبوتیک می شود.
16 سیستم آنتی ژنیک پلاکتی تاکنون شناسایی شده است، که از دو آلل a (شایع) و b (کمتر شایع) تشکیل شده است.
از این آنتی ژنها بیشتر برای تشخیص علت خونریزی های داخل جمجمه ناشی از neonatal alloimmune thrombocytopenic purpura و یا ایجاد پورپورا بعد از تزریق خون posttransfusion purpura استفاده می شود.
بیماری neonatal alloimmune thrombocytopenic purpura زمانی دیده می شود که آلو آنتی بادیهای پلاکتی مادری از طریق جفت وارد گردش خون جنین شده و با اتصال به HPA موجود در سطوح پلاکت ها ، باعث شروع پروسه همولیز و ترومبوز می شود.
دیده شده وجود بعضی از آنتی ژنها در سطح پلاکتی از جمله ژنوتایپ HPA-lb/lb واکنش پذیری بیشتری با فیبرینوژن نشان داده و درنتیجه نسبت به ژنوتایپ HPA-la/la زمینه بروز ترومبوز بیشتر می باشد.
حتی ژنوتایپ HPA-lb/lb بعنوان ریسک فاکتوری ژنتیکی برای بیماریهای عروق کرونری ( coronary artery disease = CAD) و cerebrovascular disease (CVD) محسوب می شود.